Concentratie van de zorg
Nederland brengt kankerzorg samen in Utrecht
Sinds 2024 huisvest het Utrecht Science Park, op amper één vierkante kilometer, een unieke combinatie van kennisinstellingen, (academische) ziekenhuizen en bedrijven die samen Utrecht Cancer vormen. Het gaat om meer dan 1.200 wetenschappers die er onderzoek doen naar kanker.
Filip Ceulemans

Aan de rand van de stad Utrecht ligt het Utrecht Science Park. Oorspronkelijk was hier enkel de universiteit gevestigd, maar intussen bevinden zich op de campus ook zes ziekenhuizen en meerdere start-ups. “Met 31.000 werknemers, 55.000 studenten, zes ziekenhuizen, drie kenniscentra en 17 andere instellingen en organisaties, zijn we het grootste wetenschapspark van Nederland”, zegt algemeen directeur Jan Henk van der Velden. “We brengen research, onderwijs en zorg samen. Om hier aanwezig te mogen zijn, moet je actief zijn in één van die drie domeinen.”
Een van de motoren van het Utrecht Science Park is Utrecht Cancer, waar sinds 2024 nagenoeg alle gespecialiseerde oncologische kennis van Nederland samengebracht is. “Sinds 2008 is kanker de belangrijkste doodsoorzaak in Nederland”, zegt prof. dr. Elsken van der Wall. Zij is als oncoloog voorzitter van het Strategisch Kankerprogramma van het UMC Utrecht en stond in 2024 mee aan de basis van de oprichting van Utrecht Cancer door de Universiteit Utrecht, het Hubrecht Instituut, het Prinses Máxima Centrum en het UMC Utrecht.
Brains & facilities

Het doel van Utrecht Cancer was vanaf het begin duidelijk: zoveel mogelijk expertise (‘brains & facilities’) samenbrengen om onderzoek en innovatie in kankerbehandelingen nog efficiënter te maken. “Omdat de actoren hier fysiek zo dicht bij elkaar zitten, vinden ze elkaar gemakkelijk. Zo ontstaan er dwarsverbanden en kruisbestuivingen. Fysieke nabijheid blijft een belangrijke factor, zelfs in onze digitale wereld, waar afstand irrelevant lijkt geworden.”
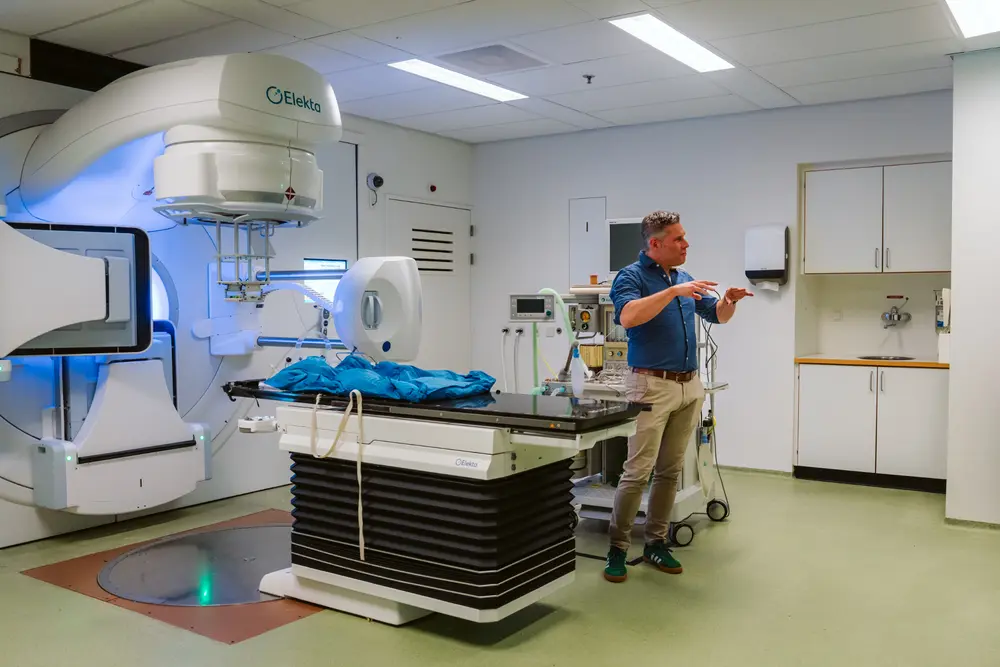
Hoewel Utrecht Cancer officieel pas in 2024 van start ging, gaat de traditie van samenwerking tussen het UMC Utrecht en commerciële bedrijven op de campus al veel verder terug. Een mooi voorbeeld daarvan is de MRI-Linac. “Wie met een MRI werkt, weet dat het verschuiven van organen in het lichaam voor problemen kan zorgen”, legt Van der Wall uit. “Samen met Elekta en Philips startten we in 1999 met de ontwikkeling van een apparaat dat een bestralingsversneller combineert met een diagnostische MRI-scanner. In 2009 stelden we het eerste prototype van de MRI-Linac voor. In 2012 en 2014 volgden nieuwe prototypes en in de zomer van 2018 namen we de eerste MRI-Linac in gebruik. Intussen wordt het apparaat wereldwijd in 98 oncologische centra gebruikt. Dankzij het toestel moeten we minder vaak opereren bij prostaatkanker. Minder ‘snijden’ betekent ook minder neveneffecten, zoals incontinentie en impotentie.”
Kinderoncologie

Een belangrijke motor achter Utrecht Cancer is het Prinses Máxima Centrum voor kinderoncologie. In het verleden telde Nederland verspreid over het land zes ziekenhuizen waar kinderen met kanker terechtkonden. Op initiatief van de ziekenhuizen zelf werd de kinderoncologie voor heel Nederland gecentraliseerd in het Prinses Máxima Centrum, dat in 2018 de deuren opende.
De centralisatie op één — weliswaar relatief centraal gelegen — locatie heeft ook impact op de ouders van oncologische patiëntjes. “Zij werden actief bij de bouw van het ziekenhuis betrokken. Zo kwamen er bijvoorbeeld kamers waar ouders kunnen verblijven, met een rechtstreekse verbinding met de kamer waar hun kind ligt. Dit is het beste ziekenhuis waar je niet wil zijn”, lacht Van der Wall.

In het Prinses Máxima Centrum ontmoeten we prof. dr. Eelco Hoving en prof. dr. ir. Jeroen de Ridder. De eerste is pediatrisch neurochirurg en klinisch directeur van de dienst neuro-oncologie, de tweede hoofdonderzoeker bio-informatica. Samen ontwikkelden ze een nieuwe technologie, Nanopore sequencing, die moet helpen om hersentumoroperaties efficiënter uit te voeren. “Een gamechanger in de oncologische chirurgie”, zeggen ze zelf.
Nanopore sequencing
“Alle Nederlandse kinderen met een hersentumor komen voor hun behandeling naar ons ziekenhuis”, zegt Hoving. “Wekelijks zijn dat er twee à drie. Vroeger wisten we voor de start van een operatie niet altijd om welke tumor het ging. Er zijn er ongeveer tachtig verschillende. In Heidelberg werd een systeem uitgewerkt om te detecteren om welke tumor het gaat, maar het resultaat liet vier dagen op zich wachten.”

“Nanopore sequencing is een technologie om DNA in real time uit te lezen”, pikt de Ridder in. “Dankzij een door AI getraind algoritme kunnen we binnen twintig tot veertig minuten het tumortype vaststellen op basis van relatief weinig materiaal. In 87% van de gevallen geeft het algoritme een correcte diagnose; in de overige 13% is er geen diagnose omdat het om een uiterst zeldzame tumor gaat. Die korte tijdspanne tussen het inleveren van tumormateriaal en het resultaat maakt het mogelijk om de chirurgische strategie meteen aan te passen aan het tumortype. In 12% van de operaties wordt de strategie ook effectief gewijzigd.”
De technologie is toepasbaar bij zowel volwassenen als kinderen. “Het belang is echter groter bij pediatrische neuro-oncologie, omdat er bij kinderen een grote variëteit aan tumoren is”, zegt Hoving. “De techniek is relatief goedkoop, wat mogelijkheden biedt voor armere landen. Doorgaans zijn er daar meer kinderen en dus ook meer tumoren bij kinderen.”
“De ontwikkeling van deze techniek is een rechtstreeks gevolg van de samenwerking die ontstaat door de aanwezigheid van diverse actoren in het Utrecht Science Park”, voegt de Ridder eraan toe. “Je hebt hier een concentratie van kennis en patiënten, en van mensen die willen samenwerken.”
Olifanten en blinde molratten
Een op het eerste gezicht misschien verrassende faculteit die bij het oncologisch onderzoek wordt betrokken, is de faculteit Diergeneeskunde. “Anders dan bij mensen is het niet onze eerste intentie om dieren met kanker te genezen, wel om de kwaliteit van hun leven te verbeteren”, zegt dr. Maurice Zandvliet, een Europees specialist in veterinaire oncologie.
Kanker bij dieren is geen uitzondering. “Eén hond op vier en één kat op drie krijgt vroeg of laat met kanker te maken”, geeft Zandvliet enkele cijfers over de incidentie bij huisdieren. “Bij honden is ongeveer de helft van de tumoren kwaadaardig, bij katten driekwart. Onderzoek naar kanker bij honden is ook voor mensen belangrijk. Sommige honden zijn immers ‘kanaries in de koolmijn’ voor bepaalde vormen van kanker bij mensen. Zo werd eerst bij dieren ontdekt dat virussen kanker kunnen veroorzaken. Door Noors onderzoek naar kanker bij Duitse herders ontdekte men genetische afwijkingen die ook bij mensen kanker kunnen veroorzaken.”
Wanneer bij een hond botkanker wordt vastgesteld, verloopt de behandeling anders dan bij mensen. “De poot wordt meteen geamputeerd, nog voor er sprake is van chemotherapie”, legt Zandvliet uit. “Dat heeft als voordeel dat we in de geamputeerde poot nog levende kankercellen hebben. Die cellen zijn beter geschikt voor onderzoek dan kankercellen die chemotherapie ondergingen, en kunnen bijdragen tot een betere behandeling van mensen met kanker.”
“Sommige dieren, zoals de blinde molrat en de olifant, ontwikkelen geen kanker. Onderzoek bij deze dieren kan ons helpen oplossingen te vinden voor mensen”, besluit Zandvliet met een opmerkelijk wist-je-datje.

