Interventionele radiologie
Cryoablatie: behandeling van de toekomst voor desmoïdtumoren
Op 5 maart voerde het team interventionele radiologie van het CHU Helora (Jolimont) de eerste cryoablatie van een desmoïdtumor uit. De patiënt maakt het goed en is zeer tevreden. Dr. Raphaël Lévêque, interventioneel radioloog, suggereert dat deze methode waarschijnlijk de standaardbehandeling zal worden, omdat deze minimaal invasief is en indien nodig herhaalbaar.
Artsenkrant: Voordat we het over de behandeling hebben, waarom horen we eigenlijk zo weinig over desmoïdtumoren?
Dr. Raphaël Lévêque: Het is eigenlijk een vrij zeldzame tumor: we hebben het over twee tot drie gevallen per miljoen inwoners per jaar. Dat gezegd hebbende, denk ik dat het aantal gevallen waarschijnlijk enigszins wordt onderschat, omdat ik er steeds vaker over hoor, vooral sinds de ontwikkeling van percutane behandelingen.
Desmoïdtumoren worden beschouwd als goedaardige tumoren: ze zijn niet infiltrerend zoals sommige sarcomen, maar ze kunnen wel erg agressief zijn. Ze worden ook wel agressieve fibromatosen genoemd. Sommige veranderen niet en veroorzaken geen of weinig hinderlijke pijn en kunnen gewoon in de gaten gehouden worden.
Maar andere groeien erg snel, en dat kan problematisch worden wanneer de tumor tegen aangrenzende structuren drukt. Op dat moment ontstaat er pijn en na verloop van tijd wordt een ingreep noodzakelijk.
Naalden voor minimaal invasieve ingrepen
Wat is in dit stadium de standaardaanpak voor interventie?
Het probleem is dat, zelfs bij een goedaardige tumor, deze zeer snel terugkeert. Chirurgisch gezien komt een interventie vaak te laat en is de tumor al behoorlijk groot. Om effectief te zijn, kan een operatie, afhankelijk van de locatie van de tumor, zeer ingrijpend zijn.
Daarom zijn er alternatieve technieken ontwikkeld, voornamelijk percutane technieken. De laatste jaren is cryoablatie bijzonder prominent geworden, en studies hebben aangetoond dat deze techniek even effectief is als een operatie, zonder de invasieve bijwerkingen.
In bredere zin zijn alle percutane thermische ablatietechnieken in opkomst, omdat er steeds meer studies, ook in toonaangevende tijdschriften, gepubliceerd worden die aantonen dat de resultaten niet onderdoen voor die van een operatie.
Hoe werkt cryoablatie precies?
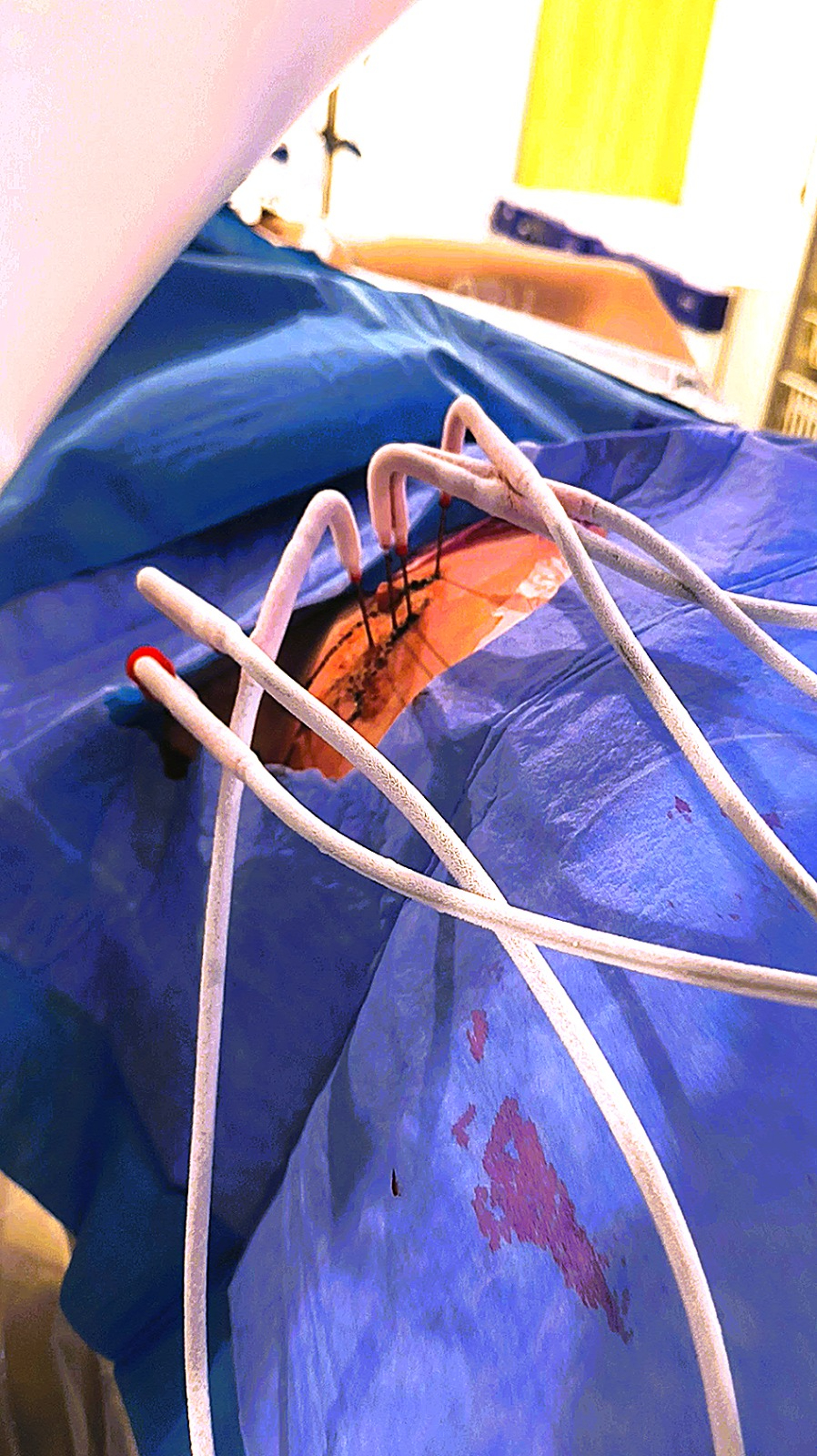
De procedure wordt uitgevoerd onder CT-scan, met sedatie of algehele verdoving, zodat de patiënt stil blijft liggen. De laesie wordt gelokaliseerd (in het geval van de patiënt die begin maart werd geopereerd, betrof het een laesie in de borstwand) en er worden meerdere naalden ingebracht. Deze naalden worden vervolgens gevuld met argongas, dat bij decompressie intense kou genereert.
Het idee is dat het 'ijsblok' groter wordt naargelang er meer naalden worden gebruikt. Afhankelijk van het type en de sterkte van de naalden kan ook een vorm gegeven worden aan dat ijsblok. Daarom is er een aanzienlijke planningsfase vlak voor de procedure. We gebruiken ook steeds meer software (soms met behulp van AI) die 3D-reconstructies en simulaties mogelijk maakt, zodat we de optimale naaldplaatsing voor het gewenste ijsblok bereiken. In het CHU Helora passen we dit soort planning ook al toe voor andere indicaties: niertumoren, levertumoren, enz. Veel start-ups begeven zich ook op dit gebied... Zelfs robotsystemen doen hun intrede.
Na de planningsfase is er tijd nodig om de naalden onder CT-geleiding correct te positioneren. Dit duurt even: ongeveer een uur voordat de naalden goed geplaatst zijn. Vervolgens starten we de koude- en warmtecycli, die elk ongeveer een half uur in beslag nemen.
IJsbal
Hoe vernietigt bevriezing de tumor?
De uiteinden van de naalden worden extreem koud en vormen een blokje ijs met een temperatuur van ongeveer -40°C. Dit wordt vervolgens licht opgewarmd om het te laten smelten. Deze afwisseling van verwarmen en afkoelen versterkt de waterbeweging in en uit de cellen, wat leidt tot celvernietiging. Dit verklaart de effectiviteit van de behandeling en induceert apoptose. De cellen 'exploderen' als het ware. Cellen die gedeeltelijk overleven, kunnen ook door deze osmotische veranderingen worden vernietigd.
Vervolgens wordt een tweede cyclus uitgevoerd, waarbij een tweede ijsblok wordt gevormd, waarna de apparatuur wordt verwijderd. Aangezien de lichaamstemperatuur 37°C bedraagt, zal het ijs geleidelijk smelten. Op de beeldvorming blijft deze 'bal' direct zichtbaar. Het toont overlapping met het bevroren gebied, dat uiteindelijk zal worden geresorbeerd. In totaal is de procedure, als alles goed gaat, in twee uur voltooid.
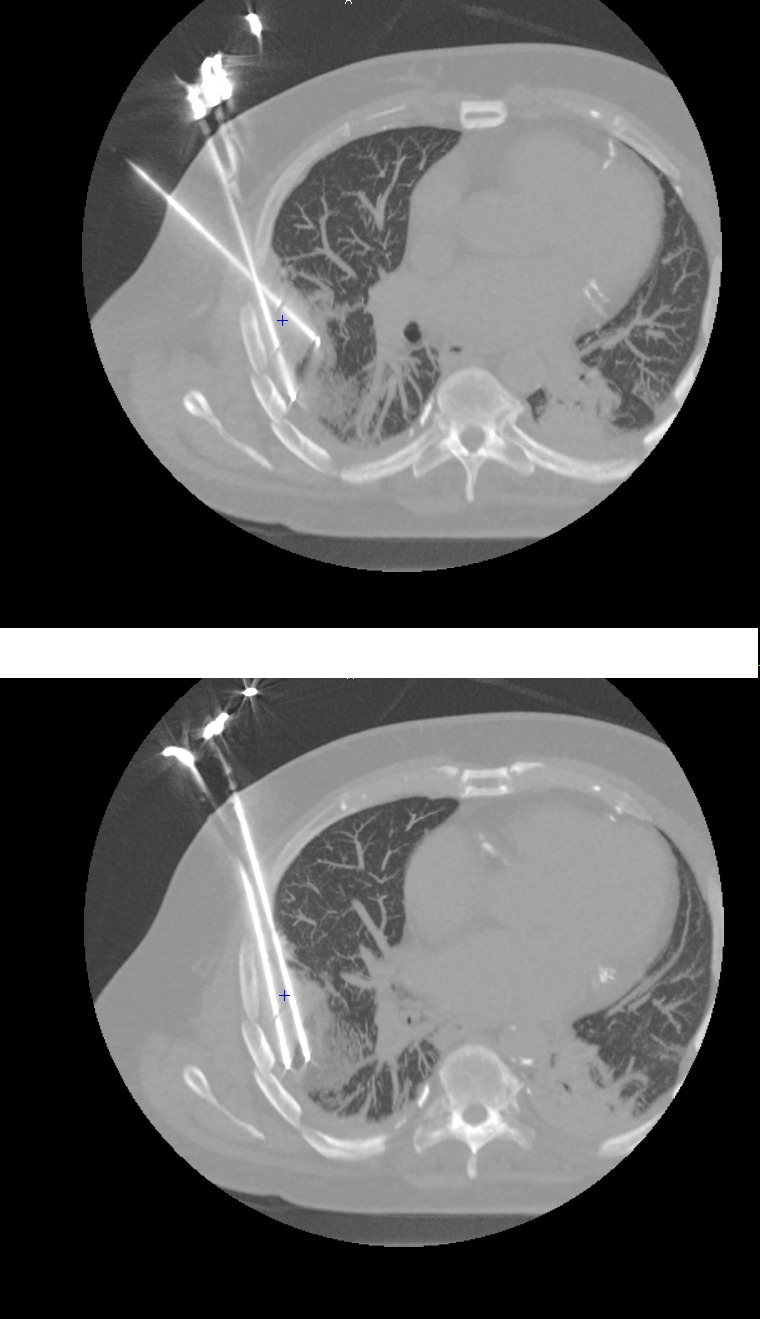
Na afloop voeren we na drie en zes maanden een vervolgonderzoek met beeldvorming uit om te controleren of de behandeling voldoende was, of dat verdere behandeling nodig is.
Logischerwijs zijn de cellen in het behandelde gebied afgestorven: we slagen erin een goede marge te behouden en, belangrijker nog, we sparen de aangrenzende structuren (zenuwen, bloedvaten) omdat we duidelijk kunnen zien waar we werken. In een geval zoals dat van onze eerste patiënt, zou het chirurgisch gezien waarschijnlijk nodig zijn geweest om een rib of zelfs een deel van het borstvlies te verwijderen: dat zou een zeer ingrijpende operatie zijn geweest.
Wat is het grote voordeel van cryotherapie?
Het belangrijkste voordeel ten opzichte van een operatie is dat het minimaal invasief kan worden uitgevoerd.
Een ander voordeel is dat er een soort 'ijsbal' (ice ball) ontstaat die duidelijk zichtbaar is op de scan: het behandelde gebied kan nauwkeurig in beeld worden gebracht en de randen kunnen worden gecontroleerd.
Het allerbelangrijkste is dat de procedure zo vaak als nodig kan worden herhaald, omdat de naalden erg klein zijn. Er zijn zelfs geen hechtingen nodig na afloop: de naalden worden ingebracht, de procedure wordt uitgevoerd en de patiënt kan meestal de volgende dag naar huis (hoewel een nacht observatie nog steeds nodig is).
In geval van problemen is een vervolgbehandeling mogelijk. Bij zeer grote tumoren kan de behandeling in meerdere sessies worden uitgevoerd.
Dit is trouwens een belangrijk punt: als je na een operatie hetzelfde gebied opnieuw moet behandelen, is er sprake van fibrose, oftewel verklevingen (in de baarmoeder "synechieën" genoemd). Chirurgen opereren liever niet opnieuw in een gebied dat al eerder is geopereerd of bestraald, omdat alles dan veranderd is. Bij cryoablatie kan je een gebied behandelen en er later terugkomen zonder dat dit een andere therapeutische optie in de weg staat.
Uiteindelijk zou men naar mijn mening cryoablatie als eerste optie moeten overwegen, en op een steeds systematischer manier. Ik denk ook dat dit geleidelijk aan zal gebeuren.
Het allerbelangrijkste is dat de procedure zo vaak als nodig kan worden herhaald, omdat de naalden erg klein zijn
Terugbetaald door RIZIV
Is de behandeling duur voor de patiënt en het ziekenhuis?
Daar zit beweging in. We zagen onze patiënt in 2025. De biopsie toonde aan dat de tumor groeide, maar in een matig tempo, dus we gaven er de voorkeur aan om af te wachten. De patiënt had geen haast met de operatie en volgens onze informatie zat de terugbetaling door het RIZIV eraan te komen. Een naald kost ongeveer € 1.200. Als we er vijf moeten gebruiken en dat wordt niet vergoed, zal de apotheek moeilijk doen. In een universitaire setting kunnen we soms met bepaalde dingen wegkomen, maar het doel is wel dat deze behandeling voor iedereen toegankelijk is.
Sinds 1 februari 2026 vergoedt het RIZIV cryoablatienaalden voor de behandeling van desmoïdtumoren in ziekenhuizen in de conventie, waaronder de site in Jolimont. Financieel gezien is het veel voordeliger dan een klassieke operatie. Patiënten hoeven niet lang in het ziekenhuis te blijven, herstellen sneller en kunnen hun activiteiten hervatten.
Er is natuurlijk één voorwaarde: de behandeling moet in gespecialiseerde centra plaatsvinden. Juist daarom heeft het RIZIV in november 2024 conventies gesloten voor thermische ablatie en percutane ablatie. In principe komt een beperkt aantal centra in aanmerking voor terugbetaling, onder voorbehoud van criteria zoals een minimum aantal uitgevoerde procedures, de beschikbaarheid van interventiemedewerkers om eventuele complicaties op te vangen en audits. Het doel is te voorkomen dat de procedure overal wordt ingezet zonder de nodige ervaring.
Patiënten hoeven niet lang in het ziekenhuis te blijven, herstellen sneller en kunnen hun activiteiten hervatten
Waarom worden niet alle solide tumoren met cryoablatie behandeld?
We moeten nog wachten op wetenschappelijke gegevens, hoewel die steeds talrijker worden. En dat is precies de reden waarom deze technieken geleidelijk aan terrein winnen in multidisciplinair overleg.
Laten we onszelf echter niet voor de gek houden: ook al is de techniek minimaal invasief, het blijft invasief. Er worden naalden ingebracht. In sommige gevallen (vooral bij een kleine, goed gelokaliseerde laesie) kan chirurgie of radiotherapie dus nog steeds de voorkeur hebben. Als interventioneel radioloog ben ik bekend met de techniek en weet ik dat er zeer weinig complicaties zijn. Ik beschouw cryoablatie over het algemeen dus als een goede optie.
Specifiek voor de lever is er in 2024 een onderzoek gepubliceerd waaruit bleek dat cryoablatie bij colorectale metastasen niet onderdoet voor chirurgie, en dat patiënten de volgende dag al naar huis konden. Uit een Deens onderzoek, gepubliceerd in 2025, bleek dat cryoablatie bij bepaalde niertumoren vergelijkbaar is met chirurgie.
Er zijn echter situaties waarin het ingewikkelder is. Als de tumor zich zeer dicht bij een bloedvat bevindt, kan de behandeling delicater zijn: in deze gevallen kan een operatie de voorkeur hebben, vooral als deze als 'eenvoudig' wordt beschouwd en een schone marge kan worden bereikt. Want zelfs als beeldvorming ons de marges toont, is er geen histologisch bewijs dat de behandeling met een 'schone marge' is uitgevoerd.
Er zijn dus nog steeds situaties waarin een operatie of radiotherapie essentieel blijft. Daarom is de beslissing noodzakelijkerwijs multidisciplinair: ze wordt genomen in overleg met de chirurg, de oncoloog en natuurlijk de patiënt, want de patiënt moet zelf de aanpak kunnen kiezen die het beste bij hem of haar past.

